

Приложение 7
Общие положения
Лекарственные средства из растительного сырья имеют сложную природу и разнообразные характеристики, в связи с чем при их производстве особую роль играет контроль исходных материалов, условий хранения и переработки.
Исходными материалами при производстве лекарственных средств из растительного сырья* могут быть необработанные растения, растительное сырье** или промежуточные продукты. Растительное сырье должно иметь требуемое качество и сопровождаться документацией для производителя промежуточных продуктов и лекарственных средств из растительного сырья. Для того чтобы убедиться в однородности состава растительного сырья, может потребоваться более подробная информация о способе его получения (выращивания). Важными факторами, влияющими на качество растительного сырья, являются выбор семян, условия выращивания и сбора. Эти факторы могут оказать влияние на стабильность готового продукта. Рекомендации в отношении системы обеспечения качества при выращивании и заготовке растений приведены в руководстве НМРС*** "Руководство по выращиванию и сбору исходных материалов растительного происхождения (Guideline on Good Agricultural and Collection Practice for starting materials of herbal origin).
________________
* В данном приложении под лекарственным средством из растительного сырья понимаются и традиционные лекарственные средства из растительного сырья.
** Термины даны по Директиве 2004/24/ЕС от 31 марта 2004 г., дополняющей Директиву 2001/83/ЕС о лекарственных средствах для использования человеком в отношении традиционных лекарственных средств из растительного сырья.
Растительное сырье (Herbal substances) - в основном, целое, разделенное и разрезанное растение, части растения, морских водорослей, грибов, лишайников в необработанной, обычно высушенной форме, но иногда и в свежем виде. Некоторые экссудаты (выделения) из растений, которые не прошли специальную обработку, также относятся к растительному сырью. В наименовании растительного сырья должны быть точно указаны используемая часть растения и ботаническое наименование по биноминальной системе.
Промежуточный продукт из растительного сырья (Herbal preparations) - продукт, полученный путем переработки растительного сырья, например, экстракцией, перегонкой, отжимом, разделением на фракции, очисткой, концентрацией или ферментацией. К промежуточным продуктам относятся измельченное или превращенное в порошок растительное сырье, настойки, экстракты, эфирные масла и вещества, выделенные в процессе переработки.
*** НМРС - комитет по лекарственным средствам из растительного сырья (Committee on Herbal Medicinal Products) Европейского агентства по лекарственным средствам (ЕМЕА - European Medicinal Agency).
Данное приложение распространяется на все исходные материалы растительного происхождения: лекарственные растения, растительное сырье и промежуточные продукты из растительного сырья.
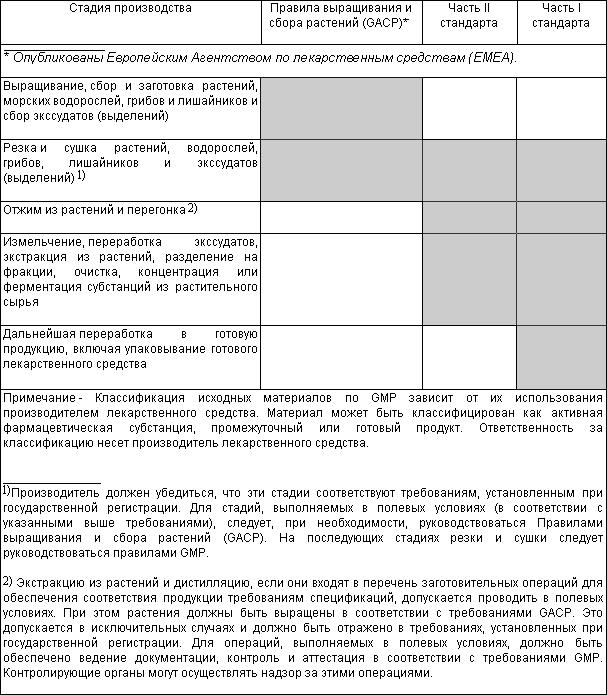
Иллюстрация применения настоящего стандарта (правил GMP) к производству лекарственных средств из растительного сырья приведена в таблице*.
________________
* Данная таблица детализирует таблицу 1 части II в отношении растительного сырья.
Помещения и оборудование
Складские зоны
1 Растительное сырье следует хранить в отдельных зонах. Эти зоны должны быть защищены от проникания в них насекомых и животных, особенно грызунов. Следует предусмотреть меры против распространения животных и микроорганизмов, привносимых с растительным сырьем, для предотвращения ферментации или роста плесени, а также против перекрестного загрязнения. Карантинное хранение поступившего растительного сырья и допущенного к использованию должно быть организовано в различных выгороженных зонах.
2 Зоны хранения должны хорошо проветриваться. Порядок размещения упаковок не должен препятствовать свободной циркуляции воздуха.
3 Особое внимание следует уделять обслуживанию и чистоте складских зон, в которых может образовываться пыль.
4 Для хранения растений, экстрактов, настоек и другой продукции могут потребоваться особые условия по влажности, температуре и освещенности, которые необходимо обеспечить и контролировать.
Производственная зона
5 При отборе проб, взвешивании, смешивании и других технологических операциях с растительным сырьем и промежуточным продуктом, сопровождающихся пылеобразованием, следует принимать особые меры по поддержанию чистоты, а также по предотвращению перекрестного загрязнения (удаление пыли, выделение специальных помещений и т.п.)
Оборудование
6 Используемое в технологическом процессе оборудование, фильтрующие материалы и пр. должны быть совместимы с растворами экстрактов, чтобы не допустить выделение и нежелательную абсорбцию веществ, которые могут оказать влияние на продукт.
Документация
Спецификации на исходные материалы
7 Производители лекарственных средств из растительного сырья должны убедиться в том, что они используют только исходные материалы растительного происхождения, соответствующие требованиям GMP и требованиям, установленным при государственной регистрации.
Следует в полном объеме вести документацию о проведении аудитов поставщиков исходных материалов растительного происхождения, выполненных производителем лекарственного средства или по его поручению. Контрольный анализ активных субстанций имеет исключительно важное значение в оценке качества исходных материалов. Производитель должен убедиться, что поставщики растительного сырья или промежуточной продукции из лекарственного сырья выполняют требования Правил выращивания и сбора растений (GACP).
8 Помимо данных, приведенных в настоящем стандарте (Часть I, раздел 4), в спецификации на растительное сырье и промежуточные продукты, используемые для производства лекарственных средств, следует включать:
- биноминальное наименование, принятое в ботанике, с указанием, при необходимости, соответствующего классификатора (например, "Классификатор растений и животных" Карла Линнея); другую информацию, например, наименование культурного сорта растения и его хемотипическую разновидность;
- подробную информацию о происхождении растения (страна или местность, и при необходимости, культура, время и способ заготовки, использование пестицидов, возможность загрязнения радиоактивными веществами и т.д.);
- указание об использовании всего растения или только его части;
- данные о методе сушки, если используются высушенные растения;
- описание растения, а также данные его макро- и микроскопического исследований;
- результаты испытаний на подлинность, в т.ч. испытания на подлинность известных активных ингредиентов или маркеров. Следует провести специальные тесты, если возникает подозрение о фальсификации или подмене лекарственного сырья; для определения подлинности необходимо иметь соответствующие образцы сравнения;
- влажность растительного сырья, определенную в соответствии с нормативным документом*;
________________
* В правилах GMP ЕС указано "в соответствии с Европейской Фармакопеей".
- по возможности, описание основных ингредиентов, обладающих установленной фармакологической активностью, или маркеров;
- методы определения содержания пестицидов и их допустимые концентрации в соответствии с нормативными документами или, при их отсутствии, аттестованным методом, если не предусмотрено иное*;
________________
* В правилах GMP ЕС указано "в соответствии с Европейской Фармакопеей".
- испытания на загрязнение грибами и/или бактериями (в т.ч. афлатоксинами, другими микотоксинами и пест-инфестацинами) и предельные значения допустимого загрязнения;
- испытания на содержание токсичных металлов и других возможных посторонних примесей;
- испытания на включение инородных материалов;
- другие виды контроля в соответствии с нормативными документами*.
________________
* В правилах GMP ЕС указано "в соответствии с общей или специальной статьей на растительное сырье Европейской Фармакопеи".
Любая обработка, обеспечивающая уменьшение загрязнений грибами, бактериями и пр., должна быть оформлена документально и включать в себя подробную информацию о процессе обработки, проводимых испытаниях и предельных значениях остаточного загрязнения.
Технологические инструкции
9 Технологические инструкции должны содержать описание различных операций, проводимых с растительным сырьем (очистка, сушка, измельчение, просеивание и пр.), а также данные о времени и температуре сушки и методах, используемых для контроля размеров фрагментов или частиц. Они также должны содержать описание методов удаления посторонних материалов (например, просеивание и пр.).
10 Особое внимание следует обратить на наличие инструкций и протоколов, удостоверяющих, что каждая упаковка тщательно осмотрена на предмет определения фальсификации, подмены или присутствия посторонних веществ (частиц металла или стекла, остатков или экскрементов животных, камней, песка и т.д.) или следов гниения или разложения.
11 Технологические инструкции должны также содержать порядок или способ удаления посторонних веществ и методы очистки (отбора) растительных материалов до помещения растительного сырья на хранение или до начала производства.
12 Инструкции по приготовлению должны содержать подробное описание растворителей, времени и температуры экстракции, стадий концентрации и методов работы.
Контроль качества
Отбор проб
13 Так как необработанное лекарственное сырье получают из отдельных растений, оно является неоднородным. Отбор проб должен проводить специально обученный персонал с соблюдением особой предосторожности. Подлинность каждой серии продукции должна быть подтверждена отдельным документом.
14 Следует сохранять контрольные образцы растительного материала, особенно, если растительное сырье не описано в нормативных документах*. При изготовлении порошков следует сохранять образцы неразмолотого растительного материала.
________________
* В правилах GMP ЕС указано "если оно не описано в Европейской Фармакопее и Фармакопее страны - члена ЕС.
15 Персонал, выполняющий контроль качества, должен иметь специальную подготовку и опыт работы с растительным сырьем, промежуточными продуктами или лекарственными средствами из растительного сырья для проведения испытаний поставляемого растительного сырья на подлинность и наличие примесей, выявления роста колоний грибов, заражения паразитами, неоднородности и т.п. в полученном сырье.
16 Подлинность и качество растительного сырья, промежуточных продуктов и лекарственных средств из растительного сырья должны контролироваться в соответствии с нормативной документацией*.
________________
* В правилах GMP ЕС указано на необходимость соответствия Европейскому руководству по качеству и спецификациям на лекарственные средства из растительного сырья и традиционные лекарственные средства из растительного сырья и, при необходимости, Европейской Фармакопее.